تشمل المذكرة اوراق عمل تقويمية علوم للصف الثامن اعاد هانم ابو العنين بإمكانكم تحميل هذا الملف على شكل بي دي إف PDF جاهز للتشغيل على أي جهاز لوحي أو إلكتروني أو كمبيوتر عن طريق زر التحميل في الأعلى, كما يمكنكم تصفح الملف فقط من خلال هذه الصفحة من الموقع مباشرة
وحدة المادة والطاقة ورقة تقويم 1
الوحدة التعليمية الاولى : المادة عنوان الدرس : ما طبيعة المادة ؟ ص 17 - ص 20
س 1 :اكمل الجدول التالي :ص 17
| وجه المقارنة | الحالة الصلبة | الحالة السائلة | الحالة الغازية |
| نوع الحركة | |||
| الحجم | |||
| الشكل | |||
| الترابط | |||
| المسافات الجزيئية |
س 2 :علل لما يأتي تعليلا علميا سليما :
1 -تتميز المادة الصلبة بشكل ثابت وحجم ثابت .
2 -تأخذ السوائل شكل الاناء الذي توضع فية .
3 -تنتشر رائحة العطر في الغرفة
س 3 :في الجدول التالي اختر من القائمة أ ما يناسبه من القائمة ب بوضع الرقم المناسب في القوسين:
| الرقم | المجموعة أ | المجموعة ب |
- المادة الصلبة . - المادة الغازية |  | |
-يمكن التمييز بين النحاس و البلاستيك. -يمكن التميز بين الحديد و الفلين. | 1 -خاصية التوصيل للحرارة و الكهرباء 2 -خاصية القابلية للطرق و السحب 3 -خاصية الطفو فوق سطح الماء | |
-الشكل الذي يوضح العلاقة بين حركة الجزيئات في المواد و الطاقة المكتسبة.
-الشكل الذي يوضح العلاقة بين المسافات الجزيئية في المواد وقوة الترابط بين جزيئاتها. | 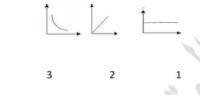
| |
| عند اضافة 300 سم من الكحول الى 300 سم3 من الماء فإن حجم المزيج يساوي تقريبا | 601 595 600 |
س 4 :اختر الاجابة الصحيحة علمياً لكل من العبارات التالية و ضع علامة √ في المربع المقابل لها:
1 - في الشكل المقابل :
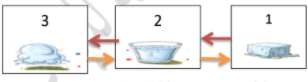
( أ ) تحول الحالة 1 إلى الحالة 2 بانخفاض درجة الحرارة وتسمى بعملية االنصهار.
(ب) تحول الحالة 3 إلى الحالة 2 بانخفاض درجة الحرارة وتسمى عملية االنصهار.
(ج) تحول الحالة.2 إلى الحالة 3 بارتفاع درجة الحرارة وتسمى عملية التجمد
(د) تحول الحالة 2 إلى الحالة 1 بانخفاض درجة الحرارة وتسمى عملية التجمد.
س 5 :ماذا يحدث في الحالات التالية:
1 - وضع كيس الشاي في كأس يحتوي على ماء ساخن
الحدث:...................................................السبب:..........................................................
2 - عند وضع العطر في زاوية المختبر.
الحدث:........................................................السبب:.......................................................
وحدة المادة والطاقة ورقة تقويم 2
الوحدة التعليمية الاولى : المادة عنوان الدرس: مم تتركب المادة ؟ ص 21 - ص 25
| العنصر | عدد البروتونات | عدد الالكترونات | عدد النيوترونات | العدد الذري | العدد الكتلي |
| C كربون | 6 | 12 | |||
| K بوتاسيوم | 19 | 20 | 39 | ||
| Si سيلكون | 14 | 24 |
مما سبق يتضح أن:
-العدد الذري = عدد...................أو = .........................
-العدد الكتلي = ...................... + ...............................
-عدد النيوترونات = العددالكتلي - عدد.......................
س 2 :علل لما يأتي تعليلا علميا سليما:
- تتركز كتلة الذرة في النواة.
- الذرة متعادلة كهربيا.
س 3 :ادرس الاشكال التالية ثم أجيب عن المطلوب

1 - العدد الذري للذرة في شكل 1 يساوي...........................
2 - المستويات التي تتحرك فيها الالكترونات بسرعة عالية تسمى..........
3 - عدد الكترونات الذرة في شكل 2 تساوي....................
4 - إذا كان العدد الكتلي للذرة في شكل1 تساوي 9 فإن عدد النيوترونات بها يساوي.....
س 4 :قم بالتوزيع الالكتروني الصحيح بالاستعانة بالعدد الذري للذرات التالية :
O 8 ذرة الاكسجين Mg12 ذرة المغنسيوم Ne 10 ذرة النيون

س 5 :أكمل المخطط التالي
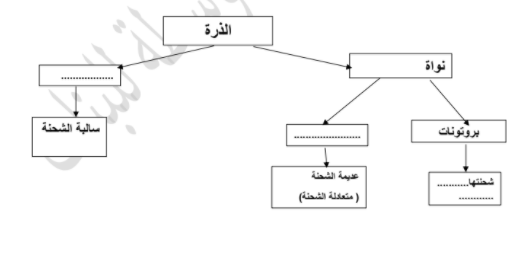
س 6 :في الجدول التالي اختر من القائمة أ ما يناسبه من القائمة ب بوضع الرقم المناسب في القوسين:
| الرقم | المجموعة أ | المجموعة ب |
-شحنة البرتون -شحنة النيوترون -شحنة الالكترون | 1 -سالبة 2 -موجبة 3 -متعادلة | |
-الذرة التي تحتوي علي نيوترونات -الذرة التي تحتوي على 4 نيوترنات. | 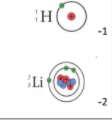 | |
_ رمز البروتون _ رمز الالكترون _ رمز النيوترون | E - 1 n - 2 p - 3
| |
-العدد الاقصى من االاكترونات التي يتسع لها المدار الاول في الذرة. - العدد الاقصى من الالكترونات التي يتسع لها المدار الثاني في الذرة |
18 8 2
|
س 7:اختر الاجابة الصحيحة علمياً لكل من العبارات التالية و ضع علامة √ في المربع المقابل لها:
1 - ذرة العنصر الموجودة بالشكل المقابل :
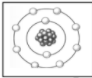
عددها الذري 8 وعدد البروتونات بها 10 عددها الذري 10 وعدد الالكترونات بها 10
عددها الذري 8 وعدد البروتونات بها 8 عددها الذري10 وعدد الالكترونات بها 8
2 - الشكل الصحيح للتوزيع الالكتروني لذرة الكلور 17 هو :
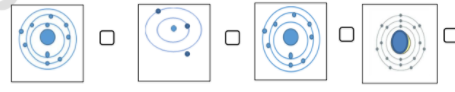
3 – عنصر عدد الكتروناته 19 وعدد نيوتروناته 20 فان عدده الكتلي يساوي:
93 39 11 27
ورقة تقويم 1
المنهج المساند : عنوان الدرس : ما هو الجدول الدوري الحديث ؟ ص 2 - ص 7
1 - رتبت العناصر في الجدول الدوري الحديث حسب الزيادة في العدد الكتلي.
2 - يحتوي الجدول الدوري على 7صفوف أفقية و 18 مجموعة رأسية.
3 - العناصر في المجموعة الواحدة تمتلك خواص كيميائية مختلفة.
4 - العناصر في الدورة الواحدة تمتلك خواص كيميائية متشابهة.
س 2:اختر الاجابة الصحيحة علمياً لكل من العبارات التالية و ضع علامة √ في المربع المقابل لها:
1 – من الرسم تقع ذرة الصوديوم في الدورة

6 5 4 3
2 – من الرسم تقع ذرة الصوديوم في المجموعة :
الاولى الثانية الثالثة الرابعة
3 – من الرسم المقابل يتضح أن ذرة هذا العنصر :
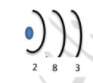
عددها الذري 13 وتقع في الدورة الرابعة و المجموعة الثالثة بالجدول الدوري
عددها الذري 13 وتقع في الدورة الثالثة و المجموعة الثالثة بالجدول الدوري
عددها الذري 13 وتقع في الدورة الثالثة و المجموعة الثانية بالجدول الدوري
عددها الذري 13 وتقع في الدورة الثالثة و المجموعة الثامنة بالجدول الدوري
4 - إذا علمتي أن ذرة عنصر ما تحتوي على 3 مستويات طاقة و عدد الالكترونات في مستواها الخارجي 6 وعددها الكتلي 32 - : فإن :
عددها الذري 32 وعدد النيوترونات بها 32 وتقع بالدورة السادسة المجموعة الثالثة بالجدول الدوري
عددها الذري 16 وعدد النيوترونات بها 16 و تقع بالدورة الثالثة المجموعة السادسة بالجدول الدوري
عددها الذري 16 وعدد النيوترونات بها 9 وتقع بالدورة الثالثة المجموعة السادسة بالجدول الدوري
عددها الذري 16 وعدد النيوترونات بها 9 و تقع بالدورة السادسة المجموعة الثالثة بالجدول الدوري
5 - العلاقة بين تدرج الخاصية الالفلزية مع زيادة العدد الذري في الدورة من اليسار إلى اليمين في الجدول الدوري :

6 -العلاقة بين تدرج الخاصية الفلزية مع زيادة العدد الذري في الدورة من اليسار إلى اليمين في الجدول الدوري :

س 3 – إذا علمت أن ذرة عنصر تحتوي على ثالث مستويات للطاقة ومستواها الثالث يحتوي علي 2 الكترون فإن :
1 - عددها الذري يساوي .............................
2 - تقع هذه الذرة في المجموعة رقم ................
3 - تقع هذه الذرة في الدورة رقم ...............
س 4 – الشكل المقابل يوضح طريقة كتابة عنصر الاكسجين في مربعات في الجدول الدوري كمثال على باقي العناصر ادرسه جيدا ثم أجيب عن المطلوب
أملء الفراغات على الرسم بالحرف المناسب لها
( أ ) اسم العنصر ( ج ) العدد الذري
( ب ) الكتلة الذرية ( د ) رمز العنصر
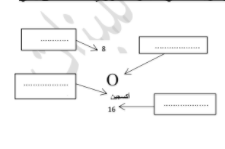
س 5 :ادرس الشكل الذي أمامك ثم أجيب عن المطلوب بإكمال الفراغات بالكلمات العلمية المناسبة:
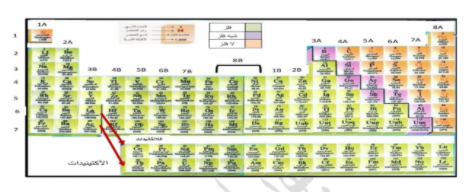
* الشكل يعرف بـالجدول الدوري الحديث حيث ترتب فيه العناصر حسب خواصها في نموذج متكرر منتظم.
1 - يتكون الجدول من 18 مجموعة رأسية تنقسم إلى ثمانية مجموعات يرمز لها بالرمز ..........و.............. مجموعات يرمز لها بالرمز B.
2 - عدد الكترونات المستوي الخارجي لذرة العنصر يدل على رقم.............
3 - عدد مستويات الطاقة في ذرة العنصر تدل على رقم ....................
4 - العدد الذري للعناصر يقل/ يزيد ................ كلما اتجهنا من اليسار إلى اليمين خلال الدورة.
5 -الخواص الفلزية تقل/ يزيد .................بزيادة العدد الذري كلما اتجهنا من اليسار إلى اليمين خلال الدورة.
6 -الخواص الافلزية )تقل/ يزيد ................ بزيادة العدد الذري كلما اتجهنا من اليسار إلى اليمين خلال الدورة.
7 - عدد مستويات الطاقة تقل/ يزيد ............ كلما اتجهنا من أعلى إلى أسفل خلال المجموعة بالجدول الدوري.
8 -تقع عناصر اللانثانيدات في الدورة ............... بينما عناصر الاكتيندات تقع في الدورة .........
9 -فسر سبب وضع عناصر اللانثانيدات و الاكتينيدات بصورة منفصلة أسفل الجدول الدوري؟
س 6:حددي في الجدول الذي أمامك موقع عنصر الكبريت مع ذكر سبب اختيارك لهذا الموقع ؟
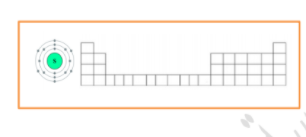
عنصر الكبريت يقع في المجموعة .....................و الدورة .......................
- السبب: ....................................
س 7 :عللي لما يأتي تعليلا علميا سليما:-
- تتشابة خواص العناصر في المجموعة الواحدة .............................
- تختلف خواص العناصر في الدورة الواحدة.

