مراجعة الاختبار القصير الأول كيمياء حادي عشر علمي ف2 #أ. إبراهيم الشهاوي 2021 2022
السؤال الأول : اكتب المصطلح العلمي الدال على كل عبارة من العبارات التالية :
| 1 | فرع الكيمياء الفيزيائية الذي يهتم بدراسة التحولات الكيميائية التي تنتج أو تمتص تياراً كهربائيا | الكيمياء الكهربائية |
| 2 | تفاعلات يحدث فيها انتقال الكترونات من أحد المتفاعلات إلى الآخر أو: تفاعلات تستخدم في استخراج المعادن من خاماتها | تفاعلات الاكسدة والاختزال |
| 3 | تفاعلات لا تنتقل فيها الكترونات من مادة لأخرى وينتج عنها مادة لا تذوب في الماء | تفاعلات التبادل المزدوج ( الترسيب) |
| 4 | عملية اكتساب الكترونات ينتج عنها نقص في عدد التأكسد | الاختزال |
| 5 | المادة التي تكتسب الكترونات وينقص عدد تأكسدها. | العامل المؤكسد |
| 6 | عملية فقد الكترونات ينتج عنها زيادة في عدد التأكسد | الأكسدة |
| 7 | المادة التي تفقد الكترونات ويزداد عدد تأكسدها. | العامل المختزل |
السؤال الأول : اكتب المصطلح العلمي الدال على كل عبارة من العبارات التالية :
1 | أنظمة أو أجهزة تقوم بتحويل الطاقة الكهربائية إلى طاقة كيميائية أو العكس من خلال تفاعلات أكسدة واختزال | الخلايا الالكتروكيميائية |
2 | خلايا تنتج طاقة كهربائية من خلال التفاعلات الكيميائية ( الأكسدة والاختزال ). | الخلايا الفولتية (الجلفانية) |
3 | ايا تحتاج إلى طاقة كهربائية وينتج منها تفاعل كيميائي من نوع الأكسدة والاختزال. | الخلايا الإلكتروليتية |
4 | الطاقة المصاحبة لاكتساب المادة للإلكترونات أي ميلها إلى الاختزال. | جهد الاختزال |
5 | جهد الاختزال عند درجة الحرارة 25°C وضغط غاز، إن وجد kPa 101 وتركيز | المحلول 1M . | جهد الاختزال القياسي |
6 | وعاء يحتوي على شريحة مغمور جزئيا في محلول الكتروليتي لأحد مرکبات مادة الشريحة . | نصف الخلية |
7 | وعاء يحتوي على شريحة مغمور جزئيا في محلول الکتروليتي لأحد مرکبات مادة | الشريحة في الظروف القياسية أي عند درجة حرارة 25°C وضغط يعادل 101kPa | وتركيز محلول 1M | نصف الخلية القياسي |
8 | قطب بلاتين مغمور في محلول حمضي يحتوي على كاتيون الهيدروجين عند ظروف قياسية. | نصف خلية الهيدروجين القياسية |
9 | میل کاتیونات الهيدروجين لاكتساب إلكترونات وتختزل إلى غاز الهيدروجين . | جهد اختزال الهيدروجين |
10 | أنبوب على شكل حرف لا يحتوي على محلول الکترولیتی مثل نیترات البوتاسيوم المذاب في جيلاتين. | الجسر الملحي |
11 | القطب السالب في الخلية الجلفانية وتحدث عنده عملية أكسدة. | الأنود |
12 | قطب الموجب في الخلية الجلفانية وتحدث عنده عملية اختزال. | الكاثود |
13 | رمز يعبر بايجاز عن الخلية الجلفانية إذ يدل على تركيبها والتفاعلات التي تحدث خلال عملها. | الرمز الاصطلاحي |
14 | مقیاس قدرة الخلية على إنتاج تيار كهربائي. | الجهد الكهربائي للخلية |
15 | حركة الالكترونات من الأنود إلى الكاثود في الخلايا الالكتروكيميائية . | التيار الكهربائي |
16 | الفرق بين جهد الاختزال لنصف الخلية الذي يحدث عنده الاختزال وجهد الاختزال النصف الخلية الذي يحدث عنده الأكسدة | جهد الخلية |
السؤال الثاني : علل لما يلي تعليلا علميا صحيحا :
1- عند وضع مسحوق خارصين في محلول كبريتات نحاس زرقاء لا يتولد تيار كهربائي ؟
لعدم وجود موصل فلزي لحركة الإلكترونات (الدائرة مفتوحة).
2- في الخلية الجلفانية يوصف الأنود بأنه سالب؟
بسبب تولد الإلكترونات عنده لحدوث عملية أكسده له
3- في الخلية الجلفانية يوصف الكاثود بأنه موجب ؟
لأنه يكتسب الإلكترونات الآتية من الأنود
4- في الخلية الجلفانية تهاجر کاتیونات الجسر الملحي نحو الكاثود والأنيونات نحو الأنود؟
لإعادة التعادل الكهربائي للمحاليل في نصفي الخلية.
السؤال الثالث: ضع علامة (✓) في المربع المقابل للإجابة الصحيحة التي تكمل الجمل التالية :
1- شروط توليد التيار الكهربائي جميع ما يلي عدا :
- ( ) وجود فرق جهد
- ( ) وجود موصل فلزي ( إلكتروني).
- ( ) وجود موصل أيوني ( الكتروليتي)
- ( ) وجود فولتميتر
2- جميع ما يلي من تغيرات تحدث عند وضع قطب خارصين في محلول كبريتات النحاس عدا واحد هو:
- ( ) تنتج طاقة حرارية
- ( ) يتغطى الخارصين بطبقة من النحاس.
- ( ) تختزل کاتیونات النحاس || .
- ( ) تنتج طاقة كهربائية .
6- جميع ما يلي من وظائف الجسر الملحي ماعدا :
- ( ) يمسح بمرور الكاتيونات إلى نصف خلية الكاثود
- ( ) يسمح بمرور الأنيونات إلى نصف خلية الأنود
- ( ) بغلق الدائرة الخارجية في الخلية الجلفانية
- ( ) يعيد التعادل الكهربائي إلى نصفي الخلية
7- جميع الخلايا الإلكتروكيميائية تحدث عملية الاختزال عند :
- ( ) القطب الموجب
- ( ) الكاثود
( ) القطب السالب - ( ) الأنود
8- في نصف الخلية القياسية يحدث جميع ما يلي عدا
- ( ) تبقى كتلة الشريحة ثابتة
- ( ) يزداد تركيز الأيونات الموجبة في المحلول.
- ( ) يعتبر نصف الخلية المفرد دائرة مفتوحة
- ( ) يبقى تركيز الكاتيونات ثابتا في المحلول .
السؤال الرابع: ضع علامة( ✓ ) أما العبارة الصحيحة وعلامة (x) أمام العبارة الغير صحيحة :
1- في جميع أنصاف الخلايا يجب أن تكون مادة الفلز من نفس نوع مادة الكاتيونات التي في المحلول. ( )
2- الجهد الكهربائي للتفاعلات التي تحدث عند شحن الخلية الجلفانية الثانوية سالب. ( )
3- يحمل الأنود شحنة سالبة في جميع الخلايا الالكتروكيميائية وتحدث عنده عملية أكسدة. ( )
السؤال السابع : الخلية الجلفانية
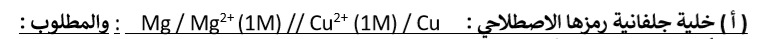
1 - أكتب نصف تفاعل الأكسدة ، نصف تفاعل الاختزال ، والتفاعل الكلي الحادث في الخلية .
نصف تفاعل الأكسدة : ............................................................................................
نصف تفاعل الاختزال : ............................................................................................
التفاعل الكلي : ............................................................................................
2 - احسب القوة المحركة الكهربائية للخلية ، علما بأن جهود الاختزال القياسية لكل من :
(المغنسيوم =2.4 - فولت ، النحاس =0.34فولت )
............................................................................................
............................................................................................

1 - ارسم شكل تخطيطي للخلية موضحا عليه كلا من الأنود والكاثود واتجاه حركة الالكترونات في السلك .
...................................................................................................................................
...................................................................................................................................
...................................................................................................................................
2 - كتابة معادلة كيميائية تمثل التفاعل الحادث عند كل من الأنود والكاثود ومعادلة التفاعل الكلي للخلية .
.....................................................................................................................
.....................................................................................................................
3- حساب جهد الاختزال القطبي القياسي لنصف خلية النيكل .
.....................................................................................................................
4- ما هو القطب الذي تزداد كتلته ويقل تركيز كاتیوناته : .....................................................................................................................
5- ما هو القطب الذي تقل كتلته ويزداد تركيز كاتیوناته : .....................................................................................................................
6- أهمية الجسر الملحي ......................................................................................................................

المطلوب:
1 - تحديد قطب الأنود وقطب الكاثود.
2 - كتابة معادلة التفاعل الحادث عند كل قطب .
3 - كتابة معادلة التفاعل الكلى الحادث في الخلية .
4 - كتابة الرمز الاصطلاحي للخلية .
5- حساب قيمة جهد الاختزال القطبي القياسي لنصف خلية الخارصين .

1 - ارسم شکلا تخطيطيا للخلية موضحا عليه كلا من الأنود والكاثود واتجاه حركة الإلكترونات في السلك .
.....................................................................................................................
.....................................................................................................................
.....................................................................................................................
2 - أكتب معادلة كيميائية تمثل التفاعل الحادث عند كل من الأنود والكاثود.
.....................................................................................................................
.....................................................................................................................
3- أكتب الرمز الاصطلاحي للخلية .
.....................................................................................................................
4 - احسب جهد الخلية القياسي .
.....................................................................................................................
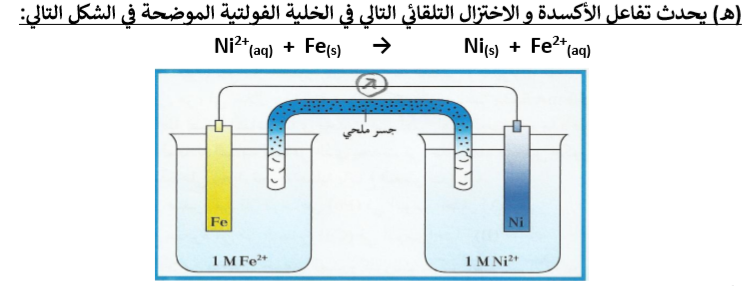
(أ)حدد الأنود والكاثود ؟
(ب) حدد الشحنات علي الأقطاب؟
(ج) اکتب نصفي التفاعل.
.....................................................................................................................
.....................................................................................................................
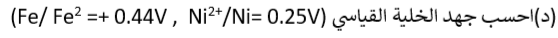
.....................................................................................................................

