مراجعة كيمياء الإيثرات للصف الثاني عشر الفصل الثاني إعداد أحمد الحسين للعام 2019
الإيثرات Ethers
هي مركبات عضوية تتميز باحتوائها على مجموعة أوكسي ( - 0 - ) كمجموعة وظيفية متصلة بشقين عضويين
الرابطة الإيثرية : هي الرابطة بين ذرة الكربون ومجموعة الأوكسي
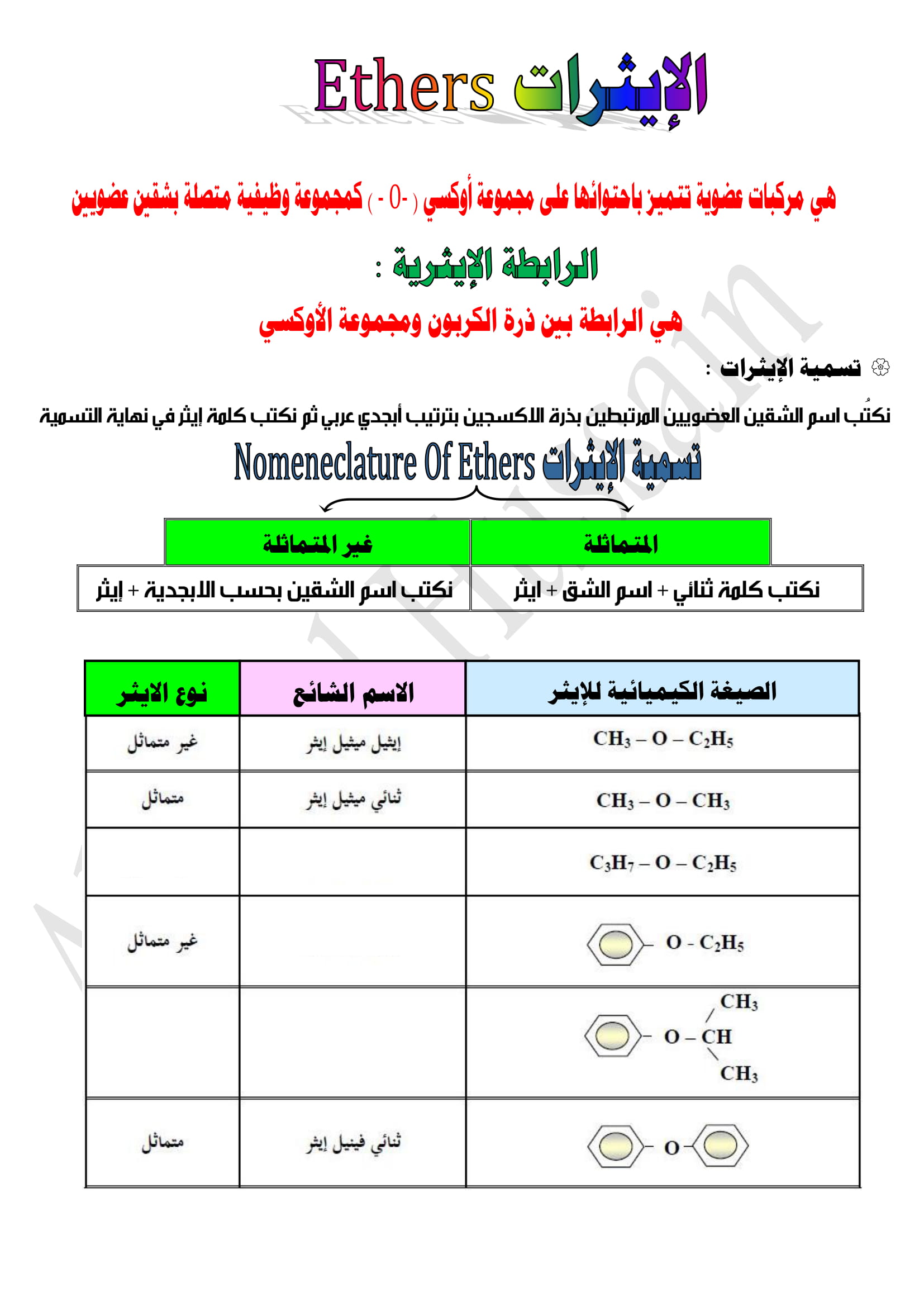
تسمية الإيثرات :
نكتب اسم الشقين العضويين المرتبطين بذرة الاكسجين بترتيب أبجدي عربي ثم نكتب كلمة إيثر في نهاية التسمية .
تسمية الإيثرات: Nomeneclature Of Ethers .
الإيثرات المتماثلة نكتب كلمة ثنائي + اسم الشق + إيثر .
الإيثرات الغير متماثلة نكتب اسم الشقين بحسب الأبجدية + إيثر .
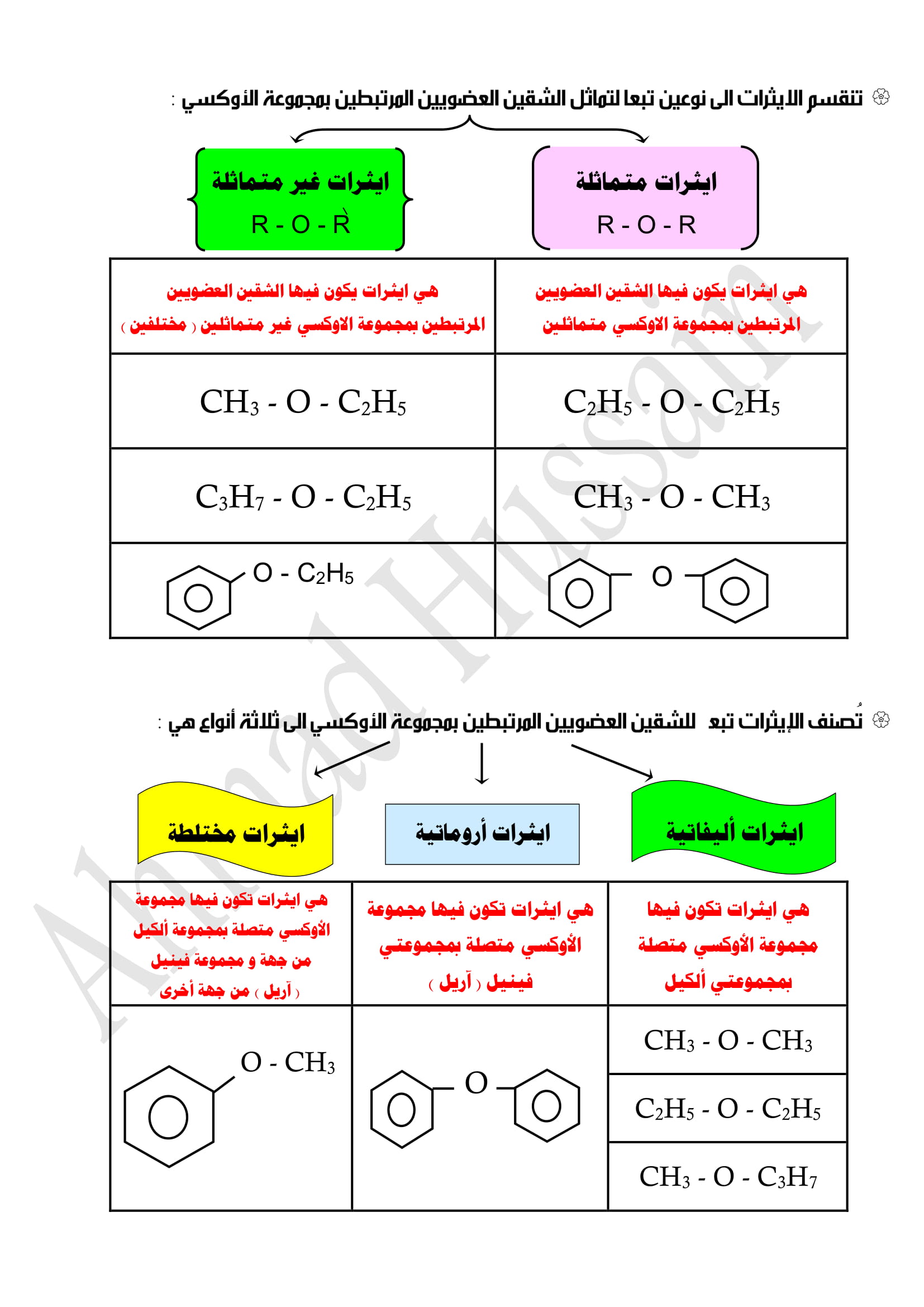
تنقسم الايثرات الى نوعين تبعاً لتماثل الشقين العضويين المرتبطين بمجموعة الأوكسي :
- إيثيرات متماثلة : هي ايثرات يكون فيها الشقين العضويين المرتبطين بمجموعة الاوكسي متماثلين .
- إيثيرات غير متماثلة : هي ايثرات يكون فيها الشقين العضويين المرتبطين بمجموعة الاوكسي غير متماثلين ( مختلفين ) .
تصنف الإيثرات تبعاً للشقين العضويين المرتبطين بوجموعة الأوكسي إلى ثلاثة أنواع هي :
- إيثيرات أليفاتية : هي إيثرات تكون فيها مجموعة الأوكسي متصلة ب مجموعتي ألكيل .
- إيثيرات أروماتية هي ايثرات تكون فيها مجموعة الأوكسي متصلة ب مجموعتي فينيل ( أريل ) .
- إيثيرات مختلطة هي ايثرات تكون فيها مجموعة الأوكسي متصلة ب مجموعة ألكيل من جهة و مجموعة فينيل ( أريل ) من جهة أخرى .
تحضير الإيثرات : Prenaration Of Ethers
يتم ذلك عند تسخين كمية وافرة من الكحول في وجود مادة نازعة للماء مثل حمض الكبريتيك حيث يتم نزع جزئي ماء من جزيئين من الكحول .
تحضير الإيثرات المتماثلة و الغير متماثلة ( طريقة ويليا مسون ) :
يتم ذلك بتفاعل هاليدات الألكيل بالاستبدال مع الكوكسيدات الفلزات مثل الكوكسيد الصوديوم حيث يحل أنيون الألكوكسيد محل أنيون الباليد .
مراجعة كيمياء الإيثرات للصف الثاني عشر الفصل الثاني إعداد أحمد الحسين للعام 2019
الخواص الفيزيائية للإيثرات Physical Properties Of Ethers
1 - علل الإيثرات مركبات قطبية ضعيفة ؟
الجواب : لوجود فرق في السلبية الكهربائية بين الكربون و الأكسجين .
2 - الإيثرات شحيحة الذوبان في الماء لكن بعض الإيثيرات البسيطة تذوب في الماء ؟
والجواب : لارتباط هيدروجين الماء بأكسجين الآيثر برابطة هجيدروجينية ضعيفة .
3 - تقل ذوبانية الإيثيرات في الماء بزيادة الكتلة الجزيئية .
4 - ذوبانية الإيثرات في الماء أقل من ذوبانية الكحولات .
5 - علل : تتميز الايثرات بدرجة غليان منخفضة نسبياً ؟
لأن جزبئات الإيثيرات لا تحتوي على مجموعة هيدرو كسيل ( ( -OH
و لذلك تتكون روابط هيدروجينية بين جزيئات الإيثر .
6 - . درجة غليان الإيثرات أقل بكثير من درجة غليان الكحولات المقاربة لها في الكتلة ؟
بسبب قدرة الكحولات على تكوين روابط هيدروجينية بين جزيناتها لوجود مجموعة القطبية بينها لا توجد هذه الروابط في الإيثيرات برغم وجود الخاصية القطبية الضعيفة فيها .
الخواص الكيميائية للإيثرات Chemical Properties Of Ethers
الإيثيرات مركبات غير نشطة كيميائياً أقل نشاطاً من الكحولات ( لا تتأثر بالعوامل المؤكسدة القوية ) .
- الإيثرات لا تتأثر بالعوامل المؤكسدة القوية أو المختزلة أو القواعد ( علل ) :
بسبب ثبات الرابطة الإيثرية التي يصعب كسرها في الظروف العادية و لضعف الخاصية القطبية في الإيثرات .
تتفاعل الإيثرات بالانشطار فقط عند تسخينها بشدة في درجات حرارة مرتفعة مع الأحماض .
استخدامات الإيثرات Uses Of Ethe
- ثنائي إيثيل إيثير سائل متطاير درجة غليانه 35 درجة يعتبر أول مخدر تم استعماله .
مراجعة كيمياء الإيثرات للصف الثاني عشر الفصل الثاني إعداد أحمد الحسين للعام 2019
و ضح بكتابة المعادلات الكيميائية الرمزية كيف نحصل على كل من :
- إيثيل بروميل إيثر من برومو الإيثان .
- أيوا بروميد ميديا إيثر من بروميل أيوا بروميل