ملخص (بخط اليد) علوم ثامن ف1
المادة
المادة : هي كل حالة كتلة و يشغل حيز من الوسط
ملاحظة :
*المادة تحتلف في صفاتها بسبب اختلاف ترتيب الجزيئات كل منها
*تتشابه في أنها جميعا تعتبر مادة مثل ( الكتب ، الهواء ، الماء )
و للمادة حالات وهي :
| الحالة الصلبة | الحالة السائلة | الحالة الغازية |
 جزيئاتها : مترابطة الحركة : اهتزازية في مكانها الحجم : ثابت الشكل : ثابت |  جزيئاتها : أقل ترابط الحركة : إنتقالية ( إنسيابية )) الحجم : ثابت الشكل : متغير ( صب الوعاء ) |  جزيئاتها : ترابط ضعيف جدا الحركة : انتقالية عشوائية ( حرة ) سريعة الحجم : متغير الشكل : متغير
|
المادة : لها خواص طبيعة مثل ( اللون ، الطعم ، الرائحة )
*توجب مواد موصلة للكهرباء و الحرارة قابلة للطرق و السحب مثل : الحديد ، النحاس ، الالومنيوم
*توجد مواد رديئة التوصيل للكهرباء و الحرارة غير قابلة للطرق و السحب مثل : الكربون ، الكبريت
البحث عن الجزئيات ص 18
1- ضع زجاجة ساعة تحتوي على قطرات من العطر في زاوية المختبر و اتركها لفترة من الزمن
الملاحظة : أختفت قطرات العطر و تنتشر الرائحة في أرجاء المختبر
فسر : جزيئات العطر سريعة التطاير و تتبخر بسرعة و تنتشر في الهواء
2- عند وضع وضع كيس شاي في كوب ماء ساخن
يتغير لون الماء إلى اللون الأحمر ( تنتشر جزيئات الشاي بين جزيئات الماء في انحاء الكوب )
تركيب المادة
المادة
| نقية | غير نقية |
| عناصر ، مركبات | مخاليط : متجانسة ، غير متجانسة |
ملاحظات مهمة
تتكون المادة سواء أكانت عناصر أو مركبات من جزيئات متشابهة أي ان جزيئات العنصر متشابهة ، جزيئات المركب متشابهة
ماالمقصود بالجزيء ؟
هو اصغر جزء في المادة و يحمل صفات و خواص المادة
جزيء العنصر يتكون من : ذرة واحدة أو ذرتين متشابهتين أو اكثر
جزيء المركب : يتكون من ذرات مختلفة لعناصر مختلفة
الذرة
تتكون من نواة و يدور حولها الإلكترونات
| نواة | إلكترونات سالبة |
بروتونات موجبة p+ نيوترونات متعادلة n+- | e- |
مما يتكون الجزيء :
يتكون من ذرة أو أكثر ( الذرات متشابهة لجزء العنصر ، ومختلفة لجزيء المركب ) (( مهم ))
مما تتكون الذرة :
تتكون من ( نواة موجبة الشحنة و نيوترونات متعادلة الشحنة ، ويدور حولها إلكترونات سالبة )
السؤال : ماذا نسمي عدد البروتونات فيها :
الجواب : عدد البروتونات يسمى ( العدد الذري ) وكل عنصر له عدد ذري معين
السؤال : ماذا نسمي مجموع أعداد البروتونات و النيوترونات في الذرة ؟
الجواب : يسمى العدد الكتلي
السؤال : كيف تتوزع الالكترونات حول النواة ؟
الجواب : توجد 7 مستويات للطاقة ولكن سوف نتناول الآن 3 مستويات
المستوى الاول يتسع ( 2 ) ويتشبع ( 2 ) إلكترون
المستوى الثاني يتسع ( 8 ( و يتشبع ( 8 ) إلكترون
المستوى الثالث يتسع ( 18 ) و يتشبع ( 8 ) إلكترون
ملاحظة : الذرة تصب رقم 8 حتى تستقر
*لكل ذرة عنصر عددا معينا من البروتونات مختلف عن ذرات العناصر الاخرى
مثال Na11 ، Mg12
السؤال : علل الذرة متعادلة كهربيا ؟
الجواب : لأن عدد البروتونات الموجبة = عدد الالكترونات السالبة
*ملاحظة : أين تتركز الذرة ؟
تتركز الذرة في النواة لوجود البروتونات و للنيوترونات و إهمال الإلكترونات
| الجسيم | الرمز | الشحنة الكهربائية |
| بروتون | p | + |
| نيوترون | n | + - |
| إلكترون | e | - |
عنصر الليثيوم
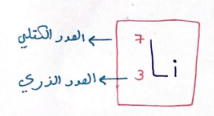
العدد الذري = 3 ـــــ هو نفسه عدد البروتونات
عدد الإلكترونات = 3 ــــــ لان عدد البروتونات = عدد الإلكترونات
عدد النيوترونات = 4 ـــــــــ عدد البروتونات - العدد الكتلي
العدد الكتلي = 7
السؤال : ما المقصود بالعدد الكتلي :
الجواب : هو مجموع أعداد البروتونات و النيوترونات اللذان يتواجدان داخل النواة